癌症细胞|ALA-CAR T平台助力白血病复发后治疗
2025-05-07 儿童肿瘤前沿 儿童肿瘤前沿 发表于陕西省
研究者通过对CD22 CAR-T细胞进行磷酸蛋白质组分析发现,低抗原刺激会导致T细胞激活连接蛋白(LAT)下游信号减弱,而LAT在T细胞信号传导中起重要作用。
CD19 CAR-T细胞在治疗复发/难治性B系急性淋巴细胞白血病(B-ALL)时,缓解率可达70~90%,但频繁复发限制了其长期疗效。复发的主要机制包括CAR-T细胞持久性不足,使得抗原阳性的B-ALL重新出现;以及靶抗原表位缺失或谱系转换导致CD19阴性复发。针对CD19阴性复发开发了CD22 CAR-T细胞,但是由于部分患者的白血病细胞CD22表达水平低于CAR-T细胞反应所需的阈值,CD22 CAR-T体内无法控制肿瘤生长。
近日,美国科罗拉多大学安舒茨医学院 Kohler 团队在 Cancer Cell 上发表题为 Restoration of LAT activity improves CAR T cell sensitivity and persistence in response to antigen low acute lymphoblastic leukemia 的研究论文。研究者通过对CD22 CAR-T细胞进行磷酸蛋白质组分析发现,低抗原刺激会导致T细胞激活连接蛋白(LAT)下游信号减弱,而LAT在T细胞信号传导中起重要作用。研究人员设计了辅助性LAT激活CAR-T细胞(ALA-CART)平台,该平台能恢复LAT活性,增强CAR-T细胞对低抗原白血病的敏感性、疗效和持久性,克服CAR-T细胞治疗失败的多种机制,且未增加毒性,是一种有前景的治疗策略。

首先,研究者通过磷酸蛋白质组学分析发现,低抗原刺激显著减少了细胞骨架重排和 MAPK信号相关的磷酸化事件,表明低抗原密度主要影响CAR-T细胞的远端信号传导,LAT 磷酸化不足和下游信号受损是CAR-T细胞对低抗原肿瘤细胞反应不佳的原因。
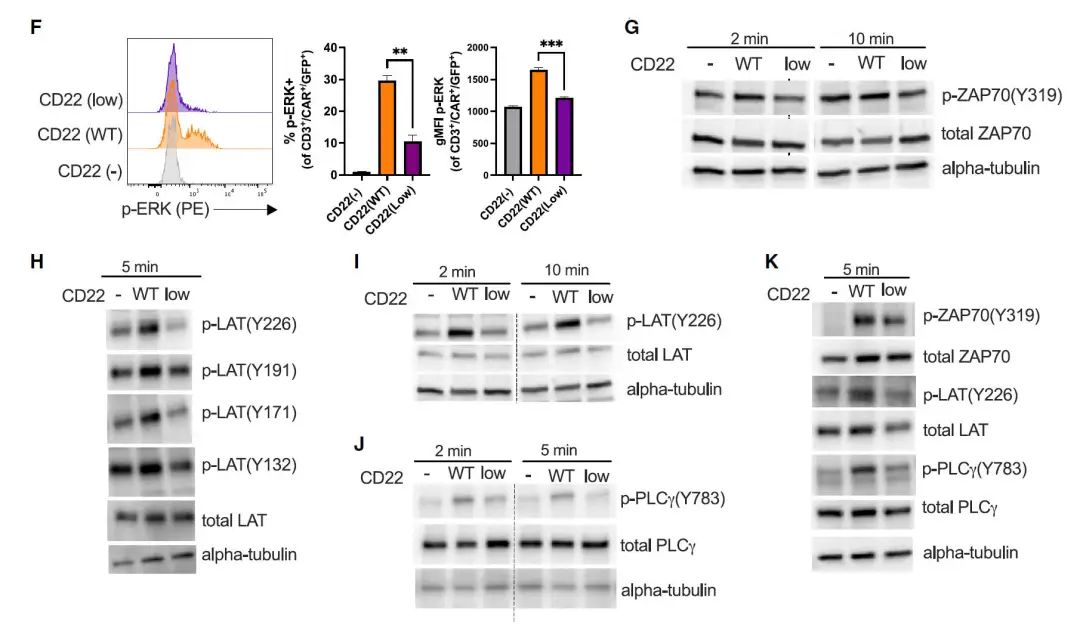
图1:低抗原刺激导致 LAT 激活效率低下,下游信号传导受损
其次,研究者构建了ALA-CART平台,22x19ALA-CART细胞同时靶向CD19和CD22,与野生型NALM6和低表达CD22 NALM6细胞共培养时,LAT-CAR的磷酸化水平更高,从而增强了PLCγ的磷酸化和体外杀伤能力。在体内实验中,22x19ALA-CART细胞可完全消除白血病细胞并延长小鼠生存时间。
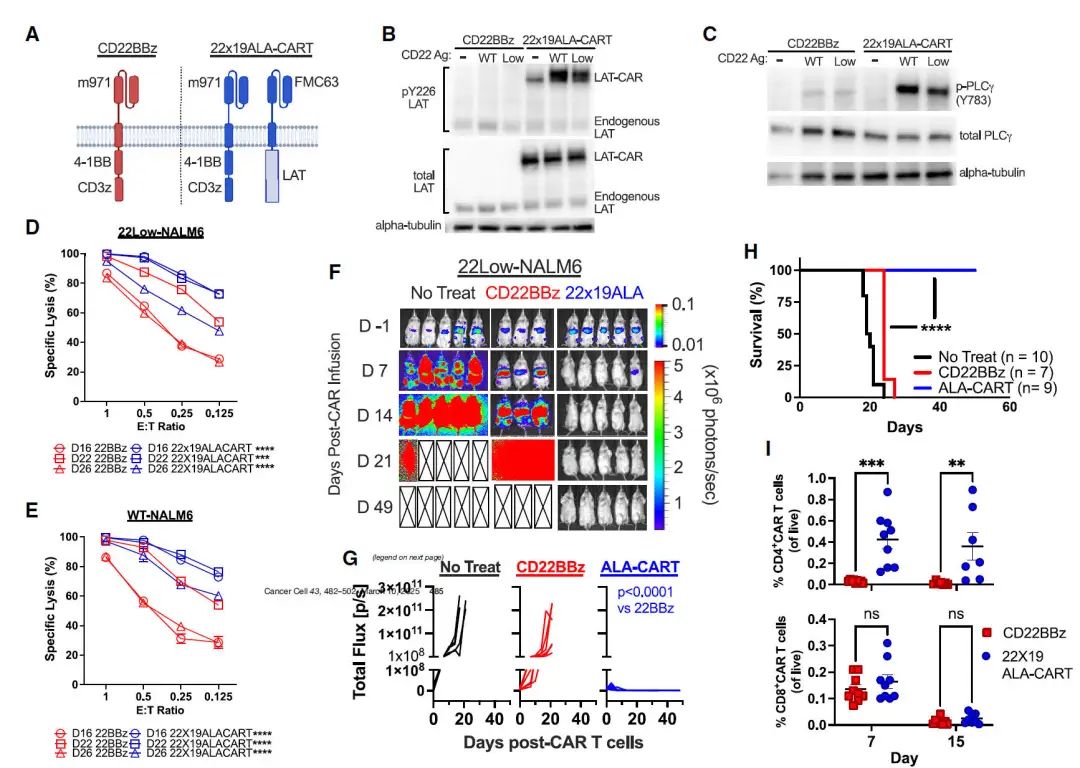
图2:22x19ALA-CART平台逆转了二代CAR-T杀伤低表达CD22白血病的功能缺陷
然后,研究者设计了单独靶向CD22的22ALA-CART,该CAR-T在体外对低表达CD22 NALM6细胞的杀伤能力增强,在体内可根除低表达CD22白血病细胞,延长小鼠生存期,在患者来源的异种移植模型中也具有良好疗效,并且该疗效提升不会引起毒性增加。
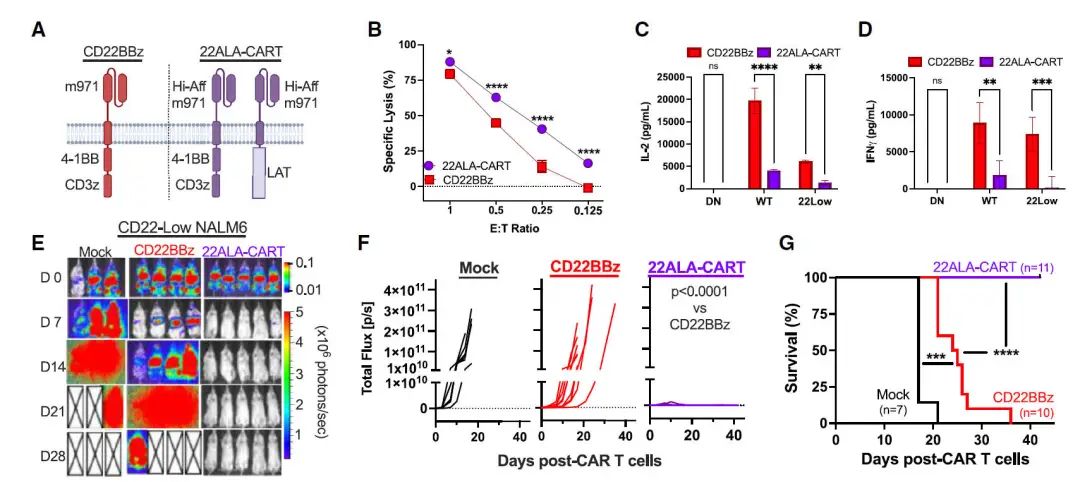
图3:ALA-CART细胞能够清除CD22低表达B-ALL细胞
最后,研究者利用转录组学测序等方式揭示了ALA-CART疗效提升的原因。通过转录组分析发现,22ALA-CART 细胞在培养后具有更少的效应T细胞分化特征,更多的幼稚T细胞特征,如更高比例的TSCM表型。而激活22ALA-CART后,细胞发生广泛的转录变化,涉及MAPK 信号通路、AP-1等。这些变化不仅影响细胞的即时功能,还改变了细胞的分化和持久性,使22ALA-CART细胞在体内具有更好的持久性。
综上所述,研究人员发现抗原低刺激会导致CAR-T细胞中LAT激活不足,影响下游信号传导,进而导致对低抗原白血病反应不佳。为解决该问题,研究人员设计了ALA-CART平台,该平台可恢复LAT活性,增强CAR-T细胞的功能和疗效,为克服CAR-T细胞治疗失败提供了新策略。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#B-ALL# #CAR-T细胞#
6