一例III期临床研究晚期食管癌病例分享
2024-06-11 网络 网络 发表于上海
ASTRUM-007研究证实免疫联合化疗治疗晚期ESCC患者具有优异疗效和可靠安全性。未来,仍需继续探索晚期食管癌免疫治疗联合模式中更优的治疗方案
食管癌是世界上最常见的癌症之一,每年发病率位于第七,死亡率位于第六1。中国是食管癌的高发地区,约90%以上为食管鳞癌(ESCC),据统计,2020年中国新增食管癌病例数为32.4万例,新增食管癌死亡病例数高达30.1万,新发病例和死亡病例均占全球半数以上2。食管癌患者预后较差,尤其是不可切除的晚期食管癌,过去以单一的治疗手段为主的治疗策略已不能满足临床诊疗需求。
随着肿瘤免疫治疗时代的到来,免疫检查点抑制剂已成为晚期食管癌的新选择和新希望3-4。其中,ASTRUM-007研究即是一项完全基于中国人群,探索PD-1抑制剂斯鲁利单抗治疗不可切除局部晚期/复发或转移性ESCC的临床研究,该研究已证实斯鲁利单抗联合化疗治疗晚期ESCC具有良好的疗效和安全性5。基于此,本期将分享一例来自ASTRUM-007临床研究中晚期食管鳞癌(ESCC)经免疫治疗后食管肿瘤消失的治疗经过,以期为广大临床医生诊疗晚期ESCC时提供思路。
病例介绍
一、基本情况
患者男性,62岁,因“进行性吞咽困难”就诊。查体:双颈部、 锁骨上窝、腋窝均未触及肿大淋巴结,剑突下上腹部轻压痛。既往史:无手术病史。家族史:否认家族遗传史。个人史:既往长期大量吸烟饮酒史。
二、辅助检查与诊断
1.胸部CT(2019-08):
检查所见:中段食管肿瘤大小约6cm,肝胃间隙转移病灶约5.5cm。
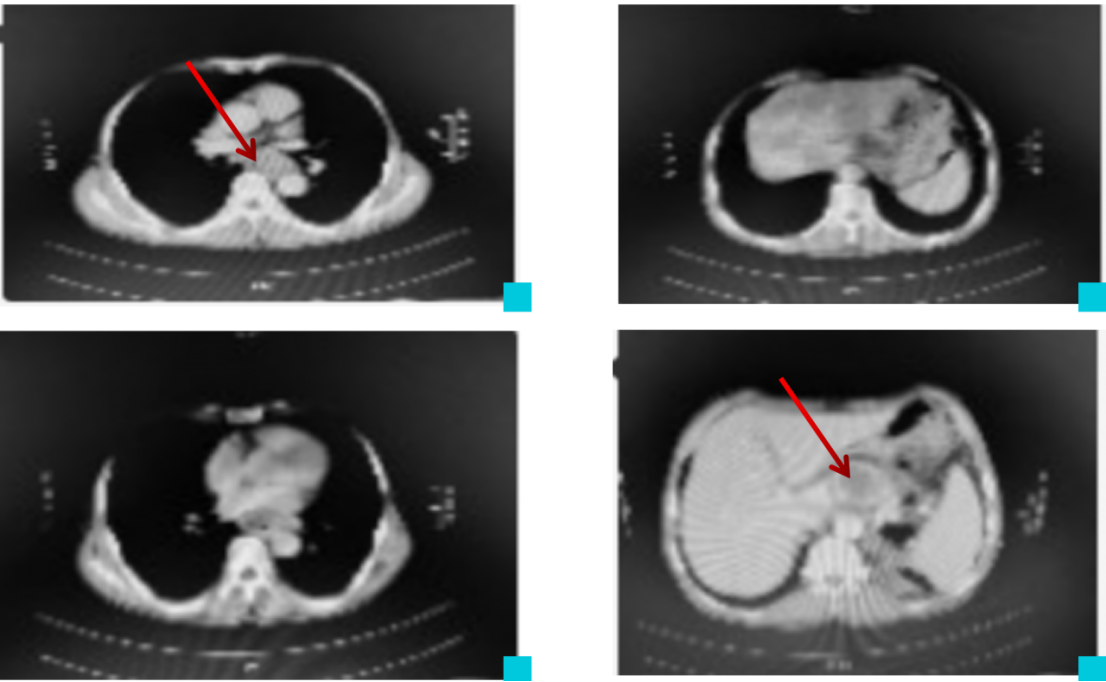
2019-08胸部CT检查
2.胃镜检查(2019-12-10)
胃镜检查所见:检查前口服链霉蛋白酶颗粒,进镜后用西甲硅油冲洗。食管距门齿26cm见一向管腔内生长的环形肿物,占据1/2及整个管腔,转换为NBI模式下观察见茶褐色区域,表面凹凸不平,粘膜充血水肿,见糜烂及溃疡形成,底披污秽苔,质硬、脆,有自发性及接触性出血,取材送检,管腔狭窄,镜身无法透过,未再继续进镜及观察全貌。
检查结论:食管Ca
病理诊断:(食管)鳞癌
活检部位:食管
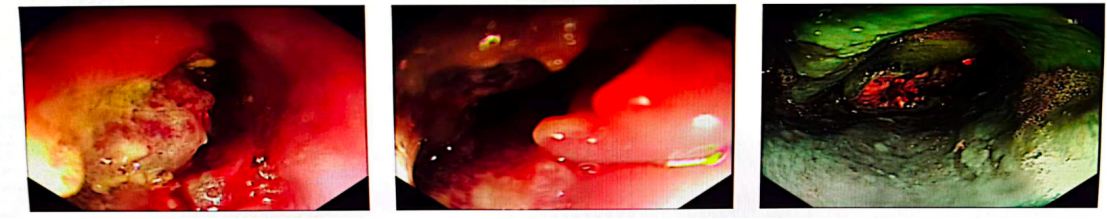
2019-12-10胃镜检查
三、治疗经过
1.入组斯鲁利单抗III期临床研究,用药方案如下:
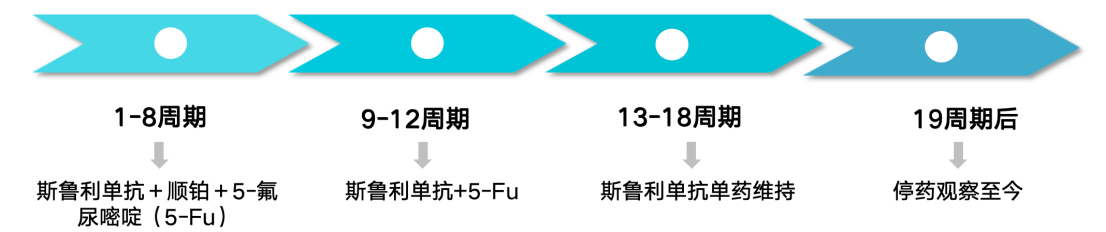
2.第一次影像学评价
治疗3周期后CT检查示:食管肿瘤及肝胃间隙转移病灶明显缩小。
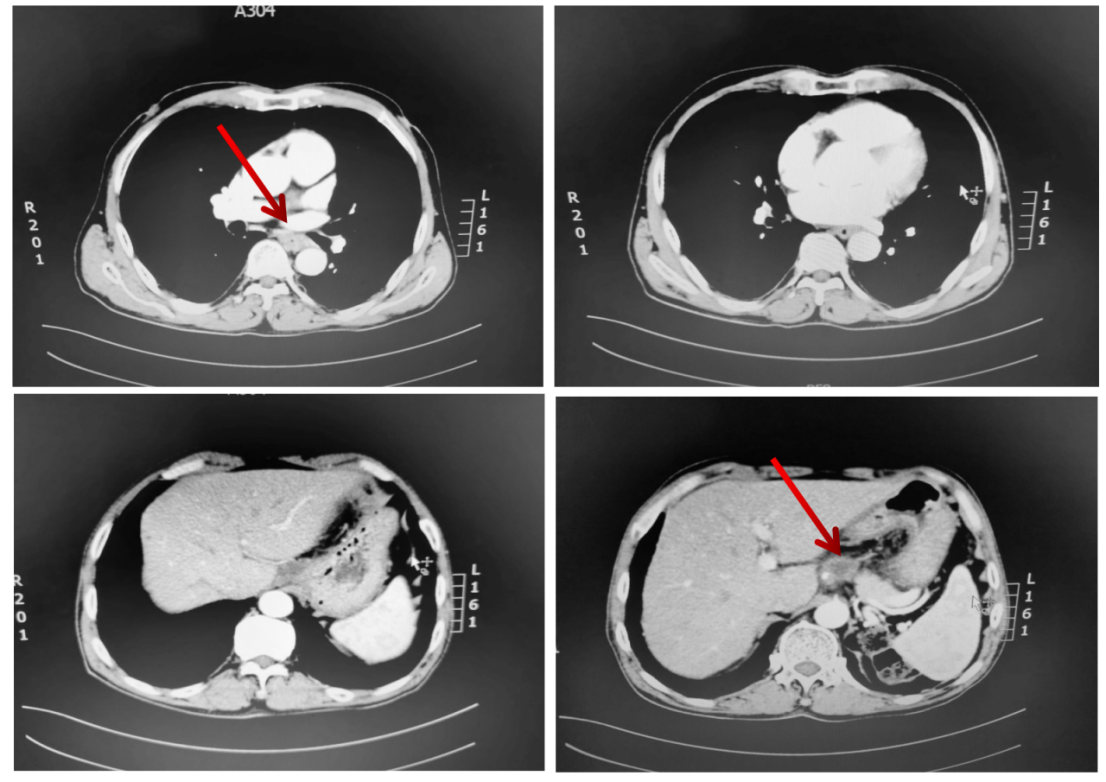
3.第二次影像学评价
治疗6周期后CT检查示:食管肿瘤及肝胃间隙转移病灶较前进一步缩小。
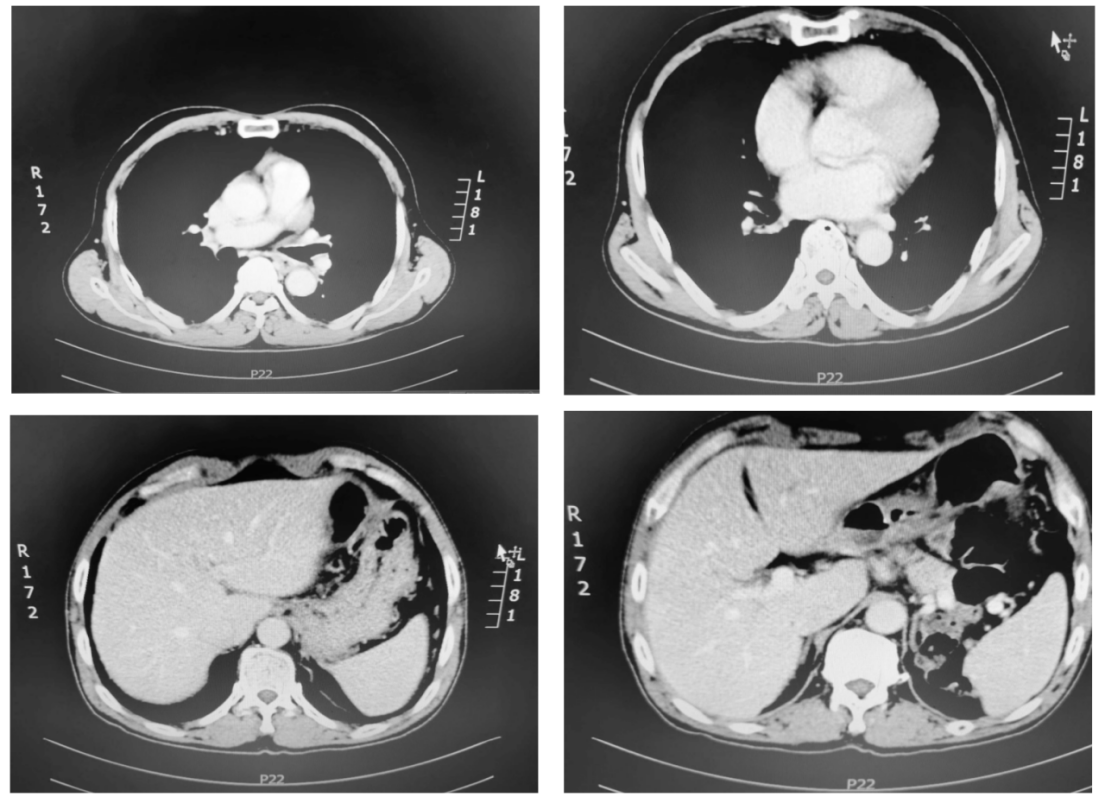
4.第三次影像学评价
1)治疗8周期后CT检查示:食管肿瘤及肝胃间隙转移病灶几乎消失。
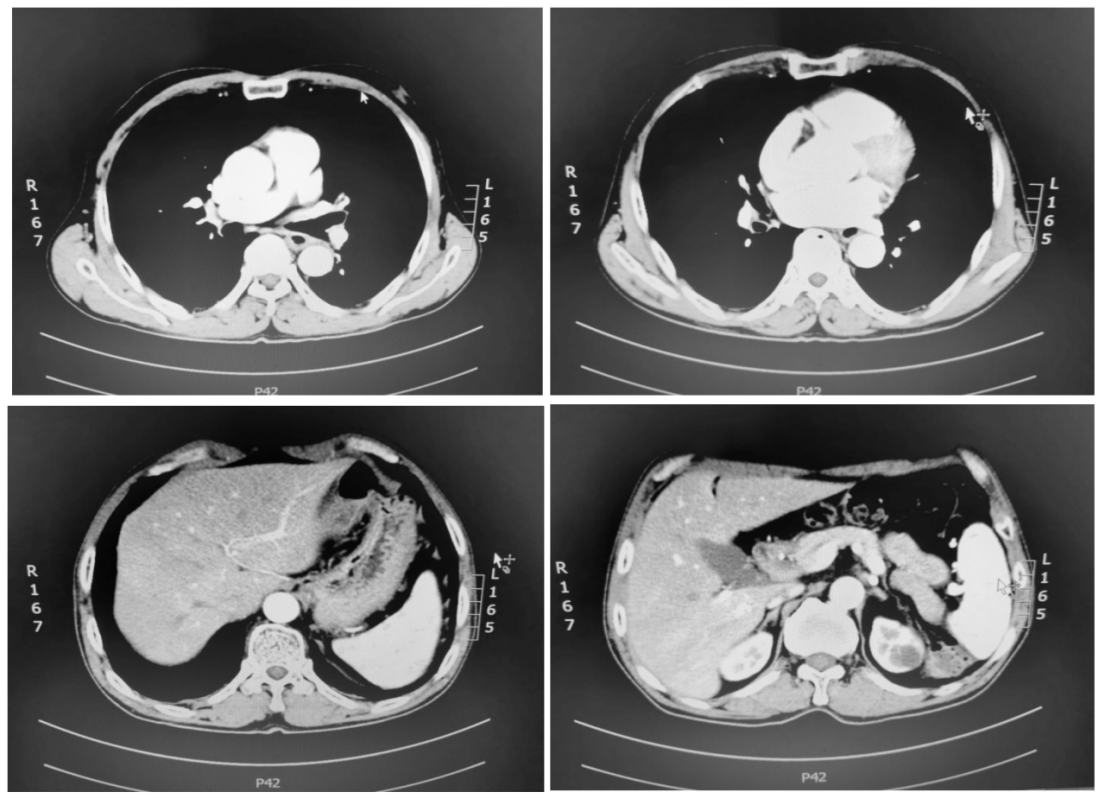
2)治疗8周期后复查胃镜示:食管粘膜未见肿瘤。
胃镜检查所见:检查前口服达克罗宁胶浆。距门齿25cm可见一憩室形成,底部光滑,NBI下观察食管余段形态及粘膜色泽未见异常。贲门开闭好,齿状线清晰。胃底粘膜未见明显异常,粘液湖浊,胃体部粘膜粗糙,花斑样改变;胃角弧形,粘膜粗糙,胃窦活动正常,粘膜变薄、粗糙,红白相间、花斑样充血,以白相为主,转换为NBI模式下观察整体呈褪色调、乏血管改变,未见茶褐色区域,延伸至胃体小弯上段,粘膜充血水肿,散在糜烂;幽门圆形,开闭好;十二指肠球部、球降交界、降段粘膜及形态正常。
检查结论:1)慢性萎缩性胃炎(C-3)伴糜烂;2)食管憩室

2021-01-08胃镜检查
5.第四次影像学评价
治疗12周期后CT检查示:稳定。
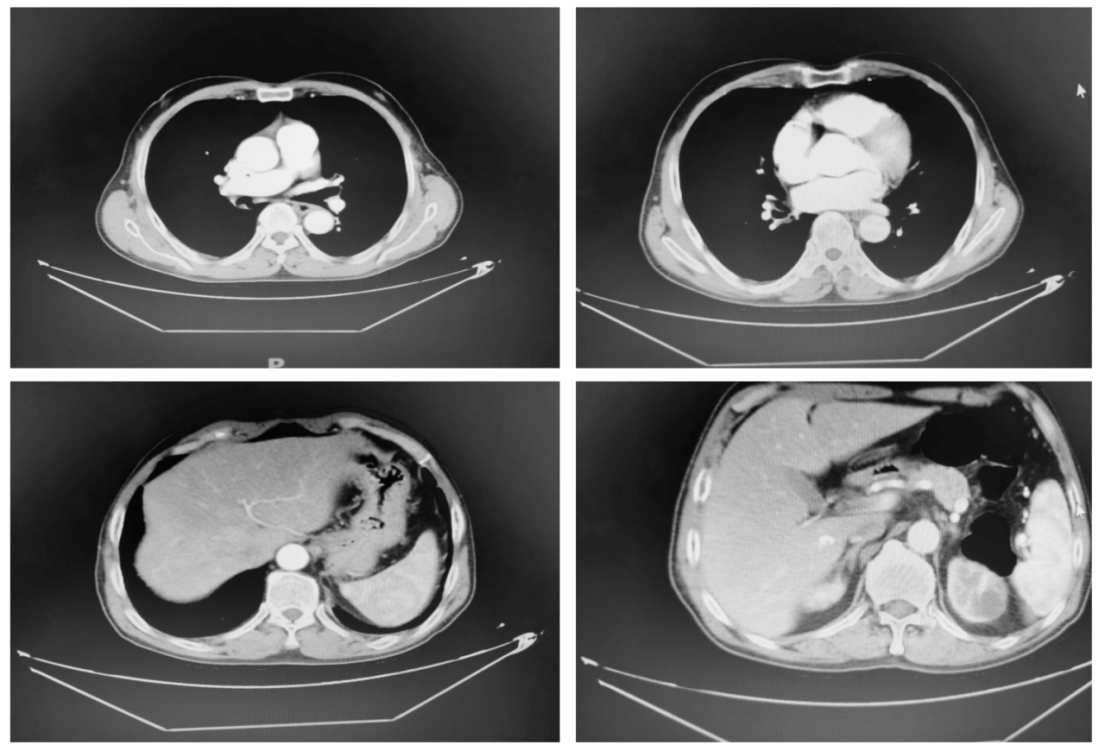
6.第五次影像学评价
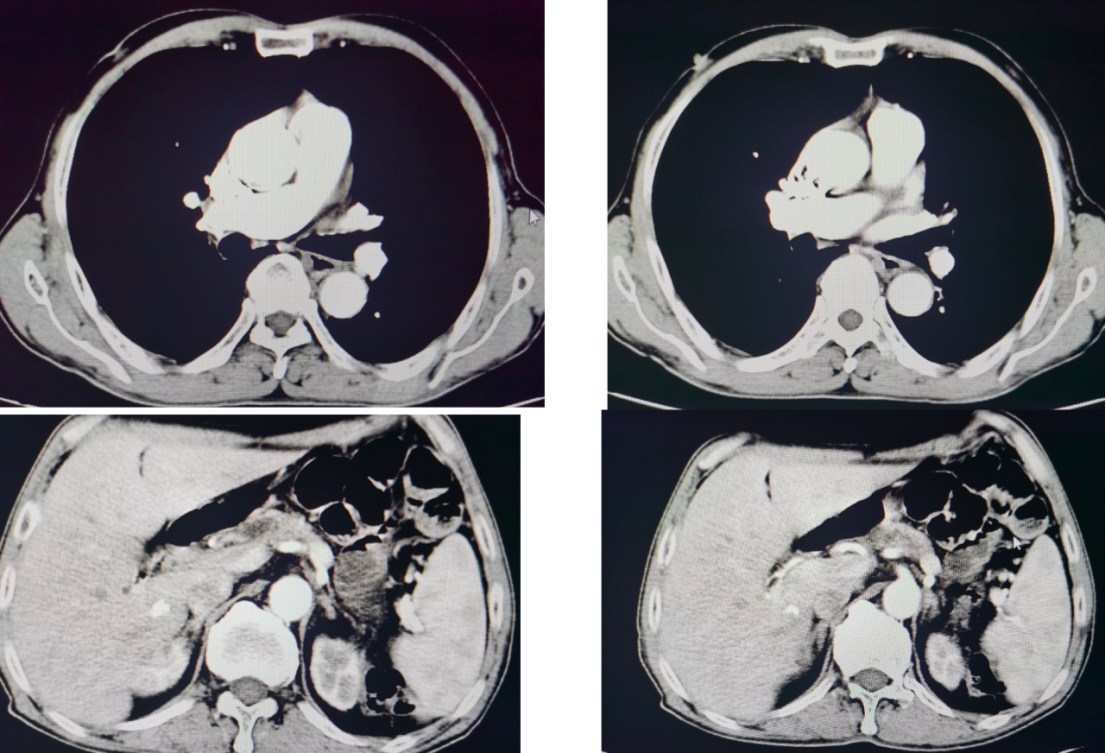
治疗18周期后CT检查示:稳定。
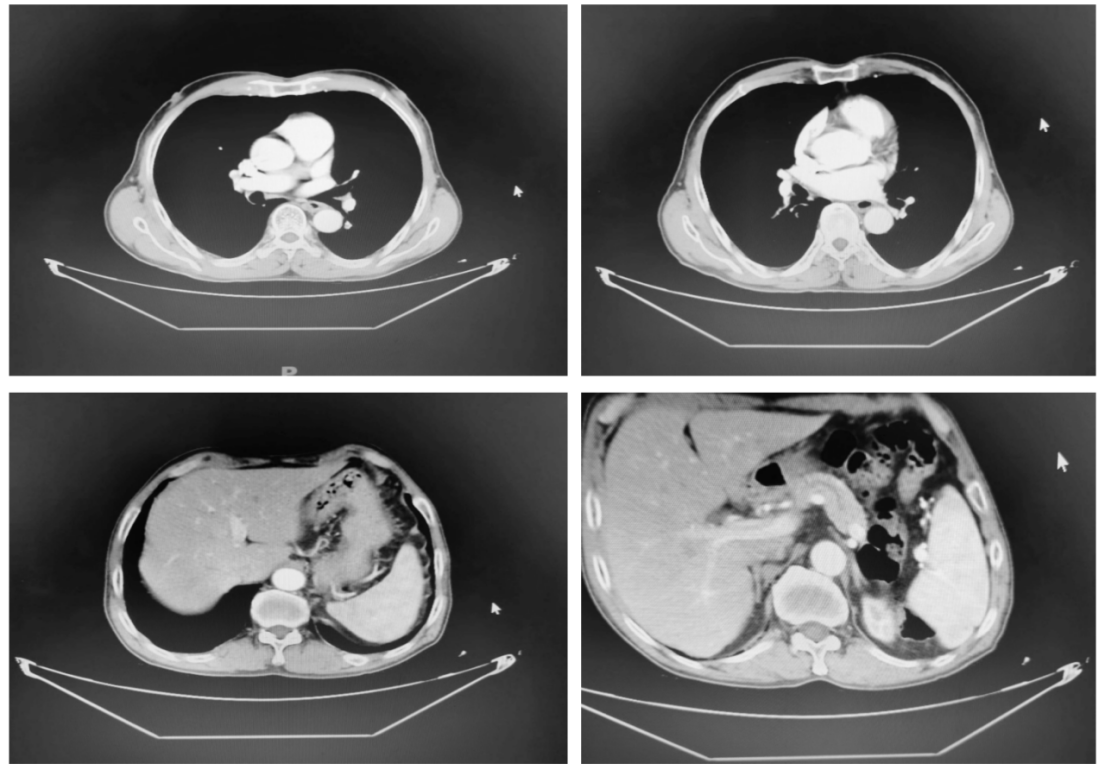
7.2023-09-07 CT检查示:稳定
8.患者治疗期间不良反应:
以1~2级不良反应为主,如肾功能不全、血小板减少症、白细胞减少和贫血等。
四、诊疗过程总结
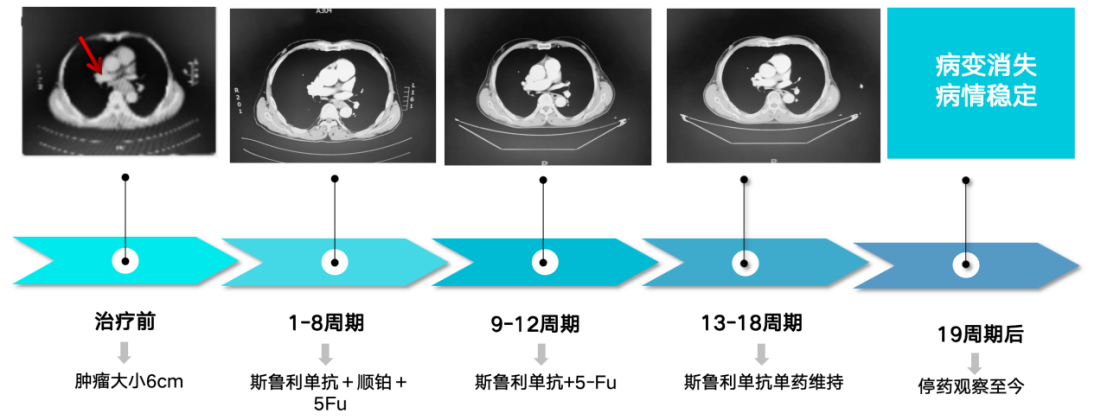
该患者在确诊晚期ESCC后,入组ASTRUM-007研究接受经斯鲁利单抗联合化疗治疗。经斯鲁利单抗+顺铂+5-Fu治疗3周期后,复查即发现食管肿瘤及肝胃间隙转移病灶明显缩小;在治疗8周期后,病灶几乎消失;12周期后病灶一直无变化,后面复查胸部CT、腹部CT均未见病灶,复查胃镜,食管肿瘤消失。期间患者不良反应较为轻微,以1~2级为主。患者每3个月行一次肿瘤评估,2023年9月的最近一次评估为病变消失、病情稳定。
讨论
近年来,随着多项临床研究证实免疫联合化疗方案为晚期食管癌患者带来了显著生存获益,免疫治疗联合化疗已成为了晚期食管鳞癌的标准治疗手段6。其中,斯鲁利单抗联合化疗方案已获得了《CSCO食管癌诊疗指南(2023年版)》的I级推荐 (1A类证据),这为国内肿瘤免疫治疗规范化提供了重要参考6。
本案例患者在确诊晚期ESCC后,在充分知情同意下,选择入组ASTRUM-007临床研究,成为该研究的重要受试者之一。该患者在完成3个周期的斯鲁利单抗联合化疗方案后,病灶即出现明显缩小,8周期后病灶几乎消失,12周后病灶稳定,这提示以斯鲁利单抗为基础的联合治疗方案抗癌效果显著。
ASTRUM-007研究是一项随机、双盲、多中心的Ⅲ期临床研究,其研究结果已发布于Nature Medicine5。研究结果显示,斯鲁利单抗联合化疗组由IRRC据RECIST v1.1评估的中位PFS和中位OS较对照组均有延长,其中,CPS≥10人群中位总生存期达到18.6个月,较对照组绝对延长4.7个月(单纯化疗组OS为13.9个月,HR=0.59[0.40-0.88]),死亡风险降低41%,疾病进展或死亡风险降低52%;此外,在客观缓解率和缓解持续时间方面,斯鲁利单抗联合化疗都展示出明显优势,其抗肿瘤活性更强,同时安全性良好5。目前,斯鲁利单抗已获得中国国家药品监督管理局(NMPA)批准上市,用于联合化疗一线治疗局部晚期/转移性食管鳞癌(ESCC)患者,这给晚期食管癌患者带来了免疫治疗新手段7。
总体而言,ASTRUM-007研究证实免疫联合化疗治疗晚期ESCC患者具有优异疗效和可靠安全性。未来,仍需继续探索晚期食管癌免疫治疗联合模式中更优的治疗方案,如与疗效更佳、安全性更高的化疗药物联合,或与其他治疗手段联合等。相信通过对治疗方案的不断探索、实践,以及对新理念和新技术的应用和推广,免疫治疗将能为中国食管癌患者带来更多获益。

宋永祥 教授,主任医师,硕士研究生导师
- 遵义医科大学附属医院胸外科主任
- 中国抗癌协会纵隔肿瘤专业委员会委员
- 中国医师协会胸外科分会手汗症专家组委员
- 吴阶平医学基金会交感神经外科专业委员会常委
- 贵州省医学会胸心血管外科分会常务委员兼秘书
- 贵州省医学会胸心血管外科分会胸腔镜学组委员
- 贵州省胸心血管外科及胸腔镜医疗质量控制中心副主任
- 贵州省抗癌协会肿瘤外科专业委员会副主任委员
参考文献:
1. Sung H, et al. Global Cancer Statistics 2020. CA Cancer J Clin. 2021;71(3):209-249.
2. 刘宇英, 魏君丽, 江柔, 伍民庆, 李艳红, 谢传波. 食管癌的流行病学及筛查研究进展[J]. 中华疾病控制杂志, 2022, 26(7): 839-844.
3.国家癌症中心,中国医师协会胸外科医师分会,中华医学会胸心血管外科学分会,等. 中国可切除食管癌围手术期诊疗实践指南(2023版).中华医学杂志,2023,103(33) : 2552-2570.
4. Obermannová R, Alsina M, Cervantes A, et al. Oesophageal cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2022;33(10):992-1004.
5. Song Y, Zhang B, Xin D, et al. First-line serplulimab or placebo plus chemotherapy in PD-L1-positive esophageal squamous cell carcinoma: a randomized, double-blind phase 3 trial. Nat Med. 2023;29(2):473-482.
6.中国临床肿瘤学会(CSCO).食管癌诊疗指南2023.
7. https://www.nmpa.gov.cn/
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言