Nature Medicine:阿尔茨海默病预测新突破,这个脑脊液指标能提前20年预警认知衰退
2025-04-07 MedSci原创 MedSci原创
这项研究不仅发现了预测AD认知预后的最佳生物标志物,更开创性地展示了血浆蛋白质组学替代脑脊液检测的可能性。
阿尔茨海默病(AD)患者认知功能衰退的速度存在巨大差异,这一直是困扰医学界的难题。虽然β淀粉样蛋白(Aβ)和tau蛋白作为AD的标志性病理指标已被广泛应用,但它们只能解释20%-40%的认知功能障碍变异。为了破解这个谜题,科学家们对来自6个大型前瞻性AD队列研究的3,397名受试者的脑脊液蛋白质组进行了分析,意外发现突触蛋白才是认知障碍最相关的生物标志物,且独立于Aβ和tau病理。这一发现可能彻底改变我们对AD认知障碍机制的理解。

研究团队运用机器学习技术,开发出一个名为CSF YWHAG:NPTX2的突触蛋白比值指标。在已经出现Aβ沉积和tau蛋白磷酸化(A+T1+)的人群中,这个指标展现出惊人的预测能力:它能够额外解释27%的认知障碍变异(相比CSF pTau181:Aβ42指标)、11%的变异(相比tau蛋白PET成像)、以及28%的变异(相比CSF神经丝蛋白、生长相关蛋白43和神经颗粒素)。更令人振奋的是,这个指标在正常衰老过程中就会发生变化,对于常染色体显性AD突变携带者,甚至能在预估症状出现前20年就检测到异常。
在长达15年的随访研究中,CSF YWHAG:NPTX2比值展现出强大的预后价值。经过多重因素校正后,该指标每增加一个标准差,A+T1+认知正常者转化为轻度认知障碍的风险就增加3倍,而轻度认知障碍进展为痴呆的风险增加2.2倍。这意味着,医生未来可能通过简单的脑脊液检测,就能准确预测哪些AD高风险人群会出现认知衰退,哪些人则能保持认知韧性,从而为个性化干预提供关键依据。
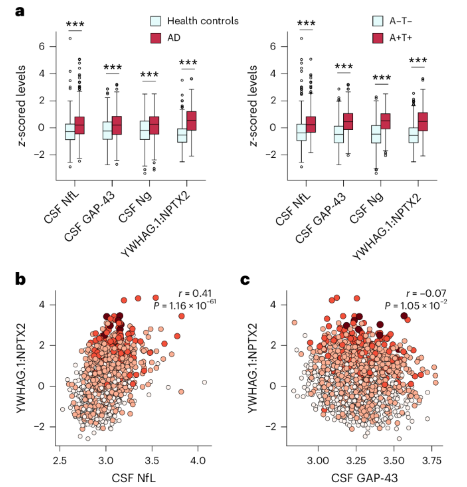
考虑到脑脊液检测的侵入性,研究团队还开发了相应的血浆蛋白质组标志物。在对13401份样本的评估中,血浆标志物部分重现了脑脊液YWHAG:NPTX2的预测效果。这一突破性进展为未来开发无创血液检测奠定了基础,有望使AD早期筛查像常规体检一样简单便捷。研究结果也再次证实,突触功能障碍是AD痴呆的核心驱动因素,为药物研发提供了新靶点。
这项研究不仅发现了预测AD认知预后的最佳生物标志物,更开创性地展示了血浆蛋白质组学替代脑脊液检测的可能性。随着这项技术的完善,我们有望建立起覆盖AD全病程的精准预测体系,从症状出现前20年就开始监测高风险人群,为早期干预赢得宝贵时间窗口。或许在不久的将来,基于这项发现的检测方法将成为临床常规,帮助更多人远离AD的威胁。
原始出处:
Oh, H.SH., Urey, D.Y., Karlsson, L. et al. A cerebrospinal fluid synaptic protein biomarker for prediction of cognitive resilience versus decline in Alzheimer’s disease. Nat Med (2025). https://doi.org/10.1038/s41591-025-03565-2
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#阿尔茨海默病# #脑脊液#
11