Eur Urol Focus:阿特珠单抗治疗未分类的局部晚期/转移性尿路癌患者的单臂国际研究 SAUL的最终结果
2024-07-05 AlexYang MedSci原创 发表于上海
美国迈耶癌症中心威尔康奈尔医学中心、意大利圣卡米洛和福拉尼尼医院等机构的研究人员评估了阿特珠单抗在未分类的尿路癌(UTC)预治疗患者中的安全性.总体而言,结果显示阿特珠单抗的耐受性良好。
近日,来自美国迈耶癌症中心威尔康奈尔医学中心、意大利圣卡米洛和福拉尼尼医院等机构的研究人员评估了阿特珠单抗在未分类的尿路癌(UTC)预治疗患者(包括通常被排除在临床试验之外的未充分研究人群)中的安全性。该研究更新了之前报告的安全性和有效性数据。

这项单臂前瞻性SAUL研究(NCT02928406)共招募了1004名局部晚期/转移性泌尿系/非泌尿系UTC患者,这些患者在晚期UTC的一至三个疗程期间/之后(或新辅助治疗后<12个月)病情进展。广泛的资格标准允许合并症复杂的患者入组,这与现实世界的情况相近。患者每3周接受一次1200毫克的阿特珠单抗治疗,直至疾病进展或出现不可接受的毒性反应。主要终点是安全性。次要终点包括反应持续时间和总生存期(OS)。
在接受治疗的患者中,10%的患者表现不佳,5%的患者肌酐清除率低于30ml/min,4%的患者患有自身免疫性疾病。中位随访期为55个月,阿特珠单抗的中位持续时间为2.8个月(0-62个月);68名患者(7%)持续使用阿特珠单抗超过4年。16%的患者发生了治疗相关的≥3级不良事件(1%死亡);8%的患者因不良事件而停用阿特珠单抗。中位OS为8.6个月(95%置信区间为7.8-9.7),136名患者(14%)的OS超过4年。
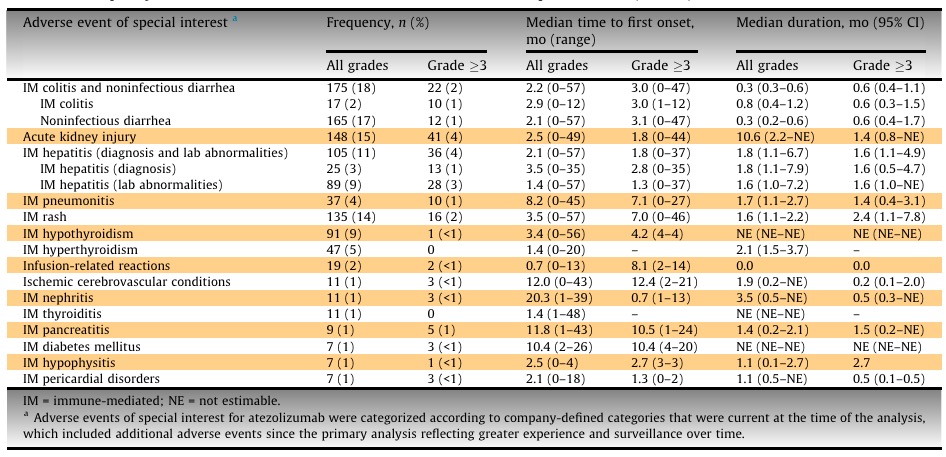
某些特别关注的不良事件的发生频率、发生时间和持续时间(N = 997)
这些关于阿特珠单抗的长期安全性和疗效的数据持续显示了阿特珠单抗可为未分类的UTC患者带来益处。值得注意的是,14%的患者在开始使用阿特珠单抗后存活了4年以上。这些结果可为多学科团队讨论和治疗决策提供参考,适用于合并症复杂的UTC患者。
SAUL研究考察了阿特珠单抗在尿路癌患者中的耐受性,这些患者之前已经接受过最多三次癌症治疗,包括通常因其他疾病而未被纳入临床试验的患者。此外,这项研究还对开始治疗后的生存期进行了评估。总体而言,结果显示阿特珠单抗的耐受性良好。
原始出处:
Sternberg CN, Loriot Y, Choy E, et al。Final Results from SAUL, a Single-arm International Study of Atezolizumab in Unselected Patients with Pretreated Locally Advanced/Metastatic Urinary Tract Carcinoma. Eur Urol Focus. 2024 Jun 4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#阿特珠单抗# #尿路癌# #转移性尿路癌#
53