【BJH】探索儿童T-ALL半相合移植的结局并建立复发的预测模型
2025-03-12 聊聊血液 聊聊血液 发表于陕西省
北京大学人民医院开展了一项回顾性研究,分析了半相合HSCT治疗儿童T-ALL的结局及复发的预后因素。
儿童T-ALL
T细胞急性淋巴细胞白血病(T-ALL)占儿童ALL病例的15%左右,通常使用与B细胞ALL(B-ALL)相似的化疗方案进行治疗。尽管传统化疗可使儿童ALL患者达到90%的5年总生存率,但T-ALL患者的预后较差,尤其是复发率较高。
近年来,CAR-T细胞疗法和贝林妥欧单抗等免疫治疗手段用于复发性ALL的治疗,但对于高危患者,造血干细胞移植(HSCT)仍是重要的治疗选择,但关于半相合造血干细胞移植的数据较少。
因此北京大学人民医院开展了一项回顾性研究,分析了半相合HSCT治疗儿童T-ALL的结局及复发的预后因素,近日发表于《British Journal of Haematology》,通讯作者为张晓辉教授和程翼飞教授。

研究结果
研究设计:该研究是一项回顾性分析,纳入2010年1月至2022年6月在北京大学人民医院接受半相合HSCT的连续T-ALL儿童患者;患者年龄≤18岁,首次接受半相合HSCT,且无既往移植史。使用以白消安(BU)为基础的预处理方案,包括阿糖胞苷、BU、环磷酰胺、抗人胸腺细胞球蛋白(ATG)等。
患者:共纳入128例患者,中位年龄12岁,74.2%为男性。从诊断到移植的中位时间为255天。
移植结果:
所有患者在移植后28天内均达到完全供者嵌合。中性粒细胞嵌合中位时间为14天,血小板嵌合中位时间为25天。
II-IV度急性移植物抗宿主病(aGvHD)的100天发生率为75.81% ± 0.14%,III-IV度aGvHD为10.40% ± 0.07%;慢性GvHD(cGvHD)的2年发生率为45.24% ± 0.24%,广泛性cGvHD为9.23% ± 0.08%。
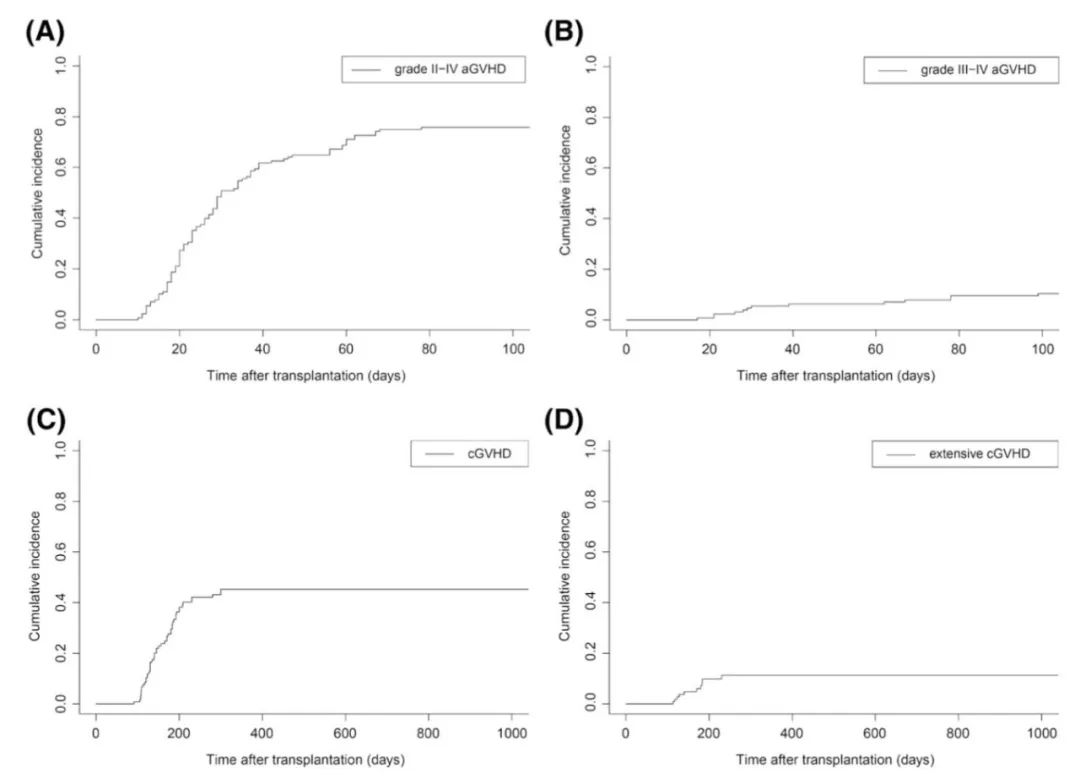
生存结果:
2年总生存率(OS)为67.77% ± 4.21%,无白血病生存率(LFS)为66.34% ± 3.82%。累积复发率(CIR)为33.82% ± 0.70%,非复发死亡率(NRM)为12.65% ± 0.46%。
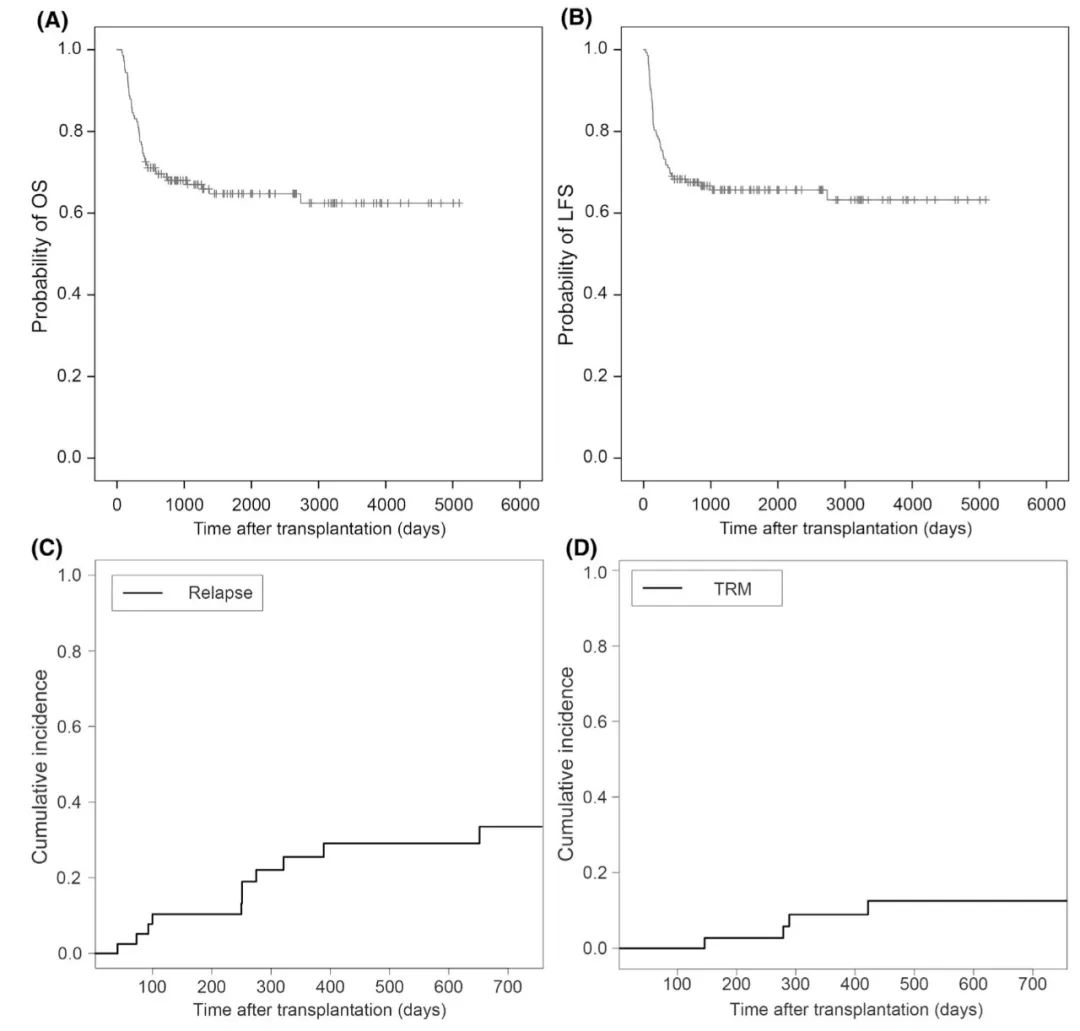
预后因素:
多因素分析显示,CD34细胞数量、移植前微小残留病(MRD)≥0.01%、无cGvHD和无巨细胞病毒(CMV)再激活与移植后复发显著相关(p<0.05)。
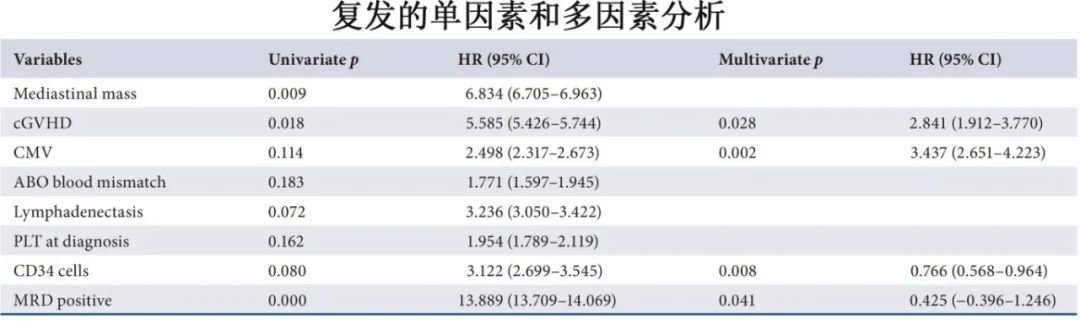
基于该四个因素开发的评分系统将患者分为低危(0-2分)和高危(3-4分)组,2年CIR分别为23.76%和48.22%(p=0.009)。
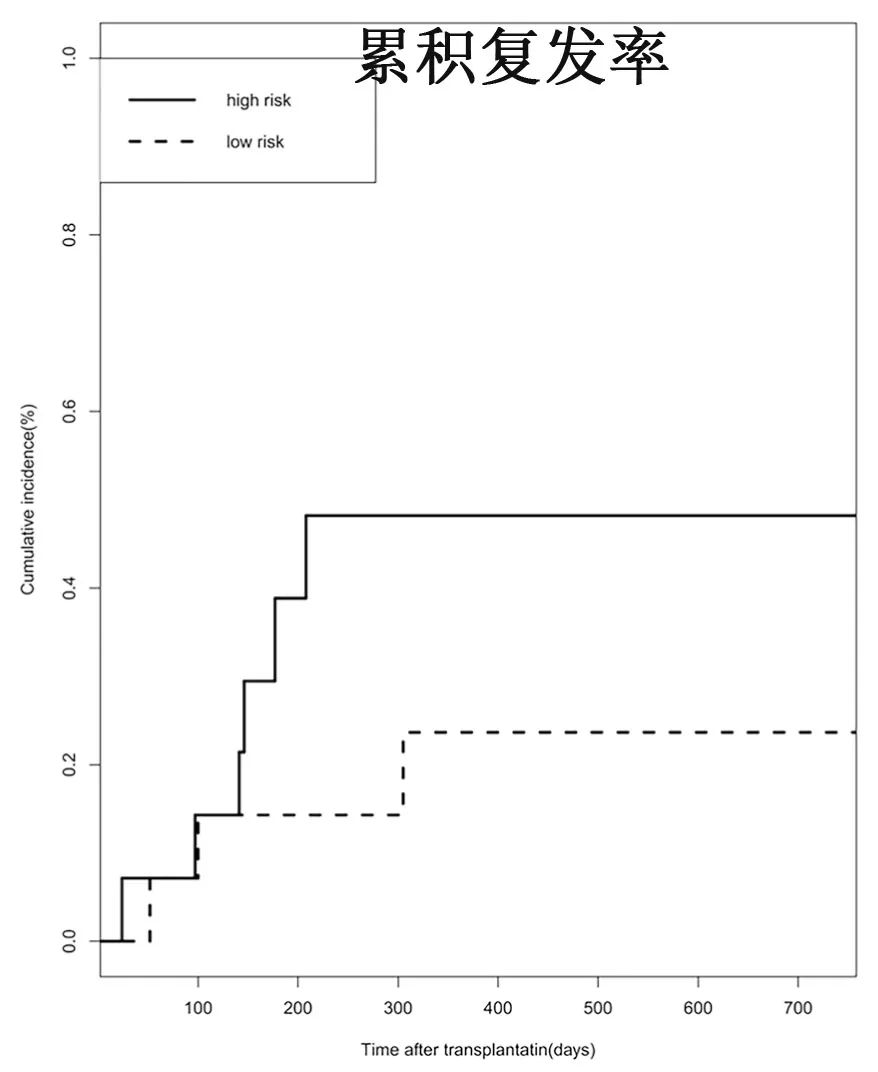
总结
半相合HSCT是T-ALL患者的有力治疗选择,但复发率仍然较高。
消除移植前MRD、保证足够数量的CD34细胞输注以及CMV感染可能是复发的保护因素。cGvHD可能通过增强移植物抗白血病(GvL)效应来减少复发。
作者开发了首个针对T-ALL患者半相合HSCT后预后的评分系统,尽管样本量较小,但该系统可用于风险分层和进一步干预的基准,该评分系统也值得进一步验证。
参考文献
Zhao C, Xiao M-Y, Zhang F, Bai L, Hu G-H, Suo P, et al. Outcomes and prognostic factors associated with relapse after haploidentical stem cell transplantation for paediatric T-cell acute lymphoblastic leukaemia. Br J Haematol. 2025; 00: 1–8. https://doi.org/10.1111/bjh.20007
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#T-ALL# #T细胞急性淋巴细胞白血病#
18